4月5日,Cell子刊《化学》(Chem)在线刊发了88038威尼斯官网主页钟芳锐教授团队和中科院生物物理所合作完成的最新研究成果“基因重构人工光敏脱卤酶全细胞催化芳卤氢/氘化”(Whole-cell-catalyzed hydrogenation/deuteration of aryl halides with a genetically repurposed photodehalogenase, DOI: /10.1016/j.chempr.2023.03.006)。该论文报道了首例人工光酶催化的脱卤还原反应,将廉价易得的芳卤类化学原料一步转化为高附加值的氘代芳烃,并且能通过基因重组的大肠杆菌进行全细胞光生物催化,具有条件温和、选择性高、底物普适性广等优点。该研究突破了天然生物酶自然进化形成的结构和功能,拓展了生物催化的反应类型和化学空间。
生物催化已经成为可持续有机合成的重要工具。然而,人类对各种非天然化学品合成的需求与自然进化形成的酶催化功能之间存在矛盾。例如,由于化学工业生产排放的一些有机卤代物的存在,自然界逐渐进化产生了降解这些污染物的细菌,在其体内已经鉴定了某些能编码脱卤酶的基因。其中,以钴胺酰胺为辅酶的还原性脱卤酶是一类重要的家族,能将电子从牺牲还原剂(如NADPH)转移还原芳基或烯基卤化物底物。然而,这些天然酶通常具有明显的底物偏好性,仅对特定底物表现出催化活性。例如,NprdhA是一种从巨大芽孢杆菌pacificus pht-3B获得的还原性脱卤酶,仅适用于2,6-二卤酚类底物。从合成化学的角度来看,芳香卤化物是合成高值精细化学品的重要原料,但目前无法通过天然进化的酶催化来实现。因此,开发底物普适性广、能高值化转化芳香卤化物的人工酶,能突破以降解为纲、底物类型专一的天然脱卤酶的功能限制,在合成生物学领域具有重要的研究意义。
钟芳锐团队致力于绿色仿生和人工生物催化领域的研究,基于化学原理驱动酶催化选择性合成的理念,发展了含有非天然光敏活性基团的人工光敏金属酶(J. Am. Chem. Soc. 2021, 143, 617)和“三重态光酶”(Nature, 2022, 611, 715),扩展了多铜氧化酶的催化杂泛性实现了非天然吲哚类底物的立体选择性氧化交叉偶联反应(Angew. Chem. Int. Ed., 2023, e202219034)。在上述人工生物催化研究基础上,团队深入开展化学和生物催化的交叉研究,利用基因密码拓展技术重构开发了含化学光催化剂的人工光敏脱卤酶(RPDase),通过捕获光子能量来驱动广谱性芳香卤化物的脱卤氢/氘化。与金属辅因子依赖性的天然脱卤酶不同,RPDase通过完全非天然的光致电子转移催化机制进行,能利用外源性甲酸钠为终端还原剂,从而避免了天然脱卤酶对还原性辅酶NADPH的依赖(图1)。
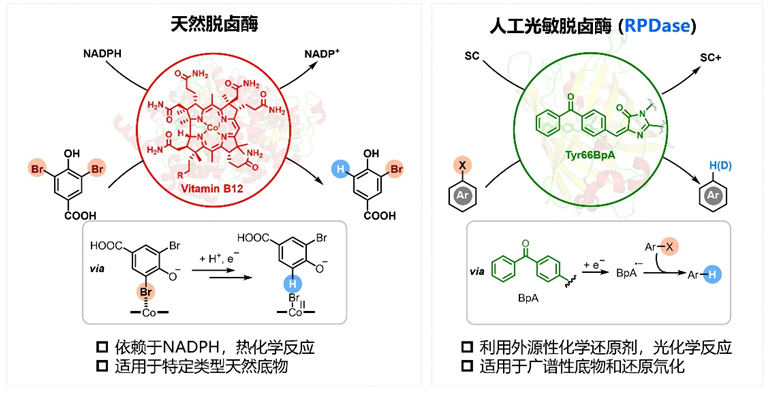
图1.天然还原性脱卤酶和人工光敏脱卤酶的对比
在优化后的反应条件下,RPDase表现了较好的底物适用性(图2)。对于吸电子基团或供电子基团取代的芳基溴化物、溴苯、4-溴苯胺、溴代吲哚、卤代吡啶及杂环芳烃、氯代芳烃、碘代芳烃、多卤素取代芳烃等30多个卤代烃底物,RPDase均能将其转化为芳烃。进一步的控制实验发现,脱卤还原的氢原子专一性地来源于甲酸钠,且不受反应液介质影响。基于这一发现,团队以氘代甲酸钠为还原剂,发展了一种专一选择性的生物催化脱卤氘化反应,并成功地应用于烟酸类似物、倍他米隆甲酯、马尿酸甲酯、沙利度胺、溴芬酸等一系列生物活性分子的氘代衍生物的制备。
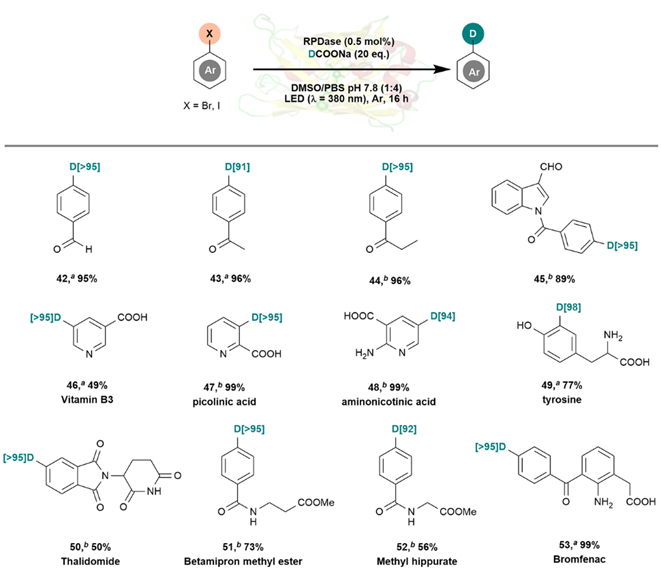
图2. RPDase催化制备生物活性分子的氘代衍生物
团队对该人工光生物催化体系的酶催化机制进行了深入探究(图3)。通过TEMPO自由基捕获、瞬态吸收光谱和电子顺磁共振等实验证明了芳基自由基的生成。同位素实验表明,甲酸钠是非常高效的终端还原剂和氢供体,氢化效率显著高于天然还原剂抗坏血酸钠。此外,开关灯控制实验发现,黑暗条件下反应会继续进行,表明反应过程中存在一定的链传递过程。基于上述实验结果,团队提出了可能的光生物催化机制。在RPDase空腔微环境中,光照和甲酸钠促使了强还原性二苯甲酮自由基阴离子和二氧化碳阴离子自由基的生成,两者均可促进芳基卤化物的单电子还原生成芳基自由基,并进一步捕获甲酸钠的氢原子或氘原子生成还原产物。
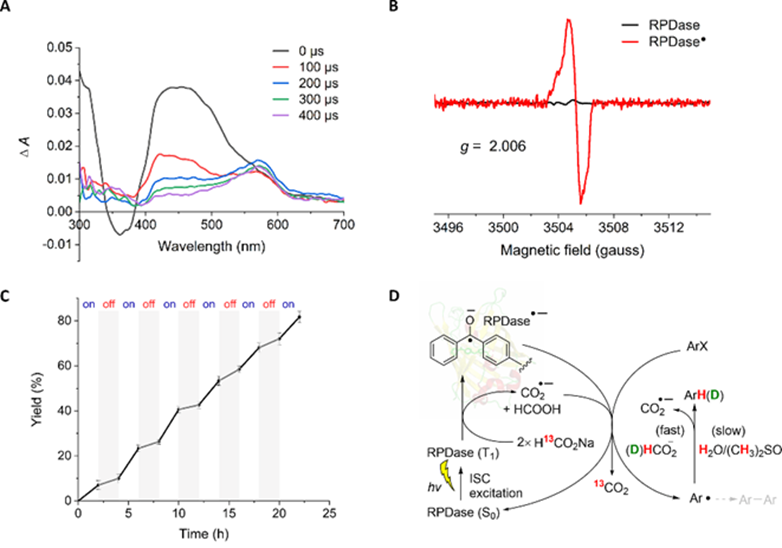
图3 RPDase光生物催化脱卤还原的催化机理研究
基于RPDase光催化的生物正交性和基因密码扩展技术,团队进一步使用表达RPDase的重组大肠杆菌细胞进行全细胞光生物催化。RPDase在活细胞条件中能同时利用内源的NADPH和外源的甲酸钠实现芳香卤化物的脱卤氢化。该研究结果表明,含有非天然光催化剂的人工光生物催化有望成为廉价易得的化学原料高值化转化的细胞工厂(图4)。
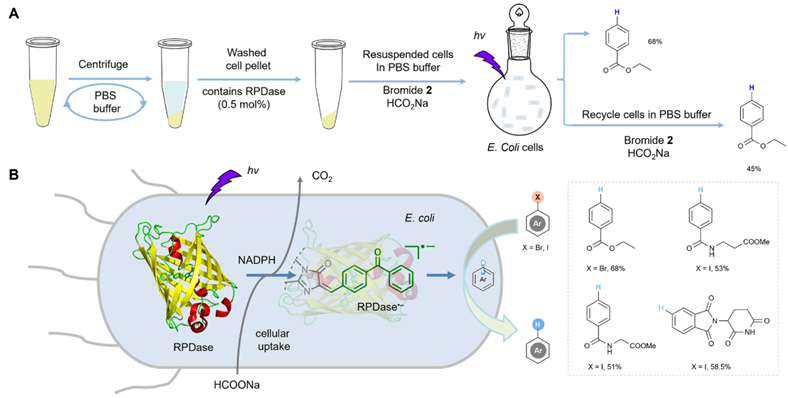
图4.全细胞光生物催化脱卤还原
该工作由88038威尼斯官网主页和中国科学院生物物理研究所合作完成。88038威尼斯官网主页钟芳锐教授和生物物理研究所王江云研究员为本文的共同通讯作者,88038威尼斯官网主页和深圳技术大学联合博士后付雨博士和生物物理研究所刘晓红研究员为本文共同第一作者。88038威尼斯官网主页为第一作者单位。该研究得到科技部重点研发计划、国家自然科学基金委、中国博士后科学基金面上项目的经费支持。
文章链接:https://www.sciencedirect.com/science/article/pii/S2451929423001250
